研究内容
有機固体のフェムト秒レーザーアブレーション
フェムト秒とは時間の単位で、1000兆分の1秒の時間をさします。光は1秒間で地球7周半(30万キロ)の距離を進むことができます。しかし、この1フェムト秒の時間で光は、300ナノメートル(nm)しか進むことができません。シャボン玉の膜の厚さが数ミクロンくらいですから、その厚さすら光が進めない時間が1フェムト秒です。フェムト秒レーザーとは、このフェムト秒の時間幅に高強度の光を集中させたパルス光のことです。
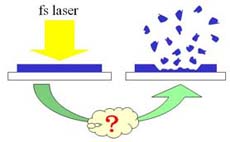
高強度のレーザーを物質に照射すると、物質が爆発的に浸蝕される現象(レーザーアブレーション)が引き起こされますが、時間的に高密度の光子が集中したフェムト秒レーザーでは、他のレーザーによるアブレーションとは異なる特殊な浸蝕現象が見られます。これまで、フェムト秒レーザーによる有機物質のアブレーションに注目して研究を進め、その特異性を示し、さらにメカニズムを明らかにしようとしています。
主な報告とトピックス
>>>PageTopフェムト秒レーザーによる細胞の非破壊操作
細胞が分散している水溶液にフェムト秒レーザーを集光し、水溶液のレーザーアブレーションにより衝撃波を発生させ、それにより細胞に力を加えて細胞を操作する方法を考案しました。レーザーを細胞に直接照射すると細胞にレーザーアブレーションが引き起こされて潰れてしまいます。一方この方法では、細胞に力学的な力のみが加わるため、細胞はレーザーによる直接的な損傷を受けません。この方法により、特定の動物細胞・植物細胞を破壊せず、操作することに成功しました。
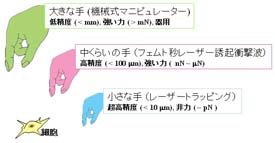
いまバイオテクノロジーにおいて、ナノメートルからミリ、センチメートルにわたる幅広い領域で細胞を操作する“手”が必要とされています。そのためには、レーザートラッピングよりも少し操作精度が劣っても、機械式のピンセットよりも少し弱いくらいの力で細胞を操作できる“手”が必要です。フェムト秒レーザーによる“手”は、まさにこの様な特徴を持っており、機械式マイクロピンセット、レーザーピンセットと併用することにより、細胞レベルから生体組織レベルまでのバイオ試料を自由に扱えるようになると期待しています。
主な報告とトピックス
>>>PageTopフェムト秒レーザーによる結晶化誘起
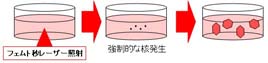
有機分子やタンパク質の過飽和溶液にフェムト秒レーザーを集光照射することで、これらの結晶化を誘起することに、世界で初めて成功しました。タンパク質や有機超分子の機能を調べる上で、分子の形(分子構造)を明らかにすることが不可欠です。そのためには単結晶が作製され、その構造を放射光(X線)を用いることにより解析することが不可欠です。現在、播磨科学公園都市にあるSPring-8のような高輝度放射光施設を用いることにより、数10ミクロンの高品質単結晶が作製できれば、その分子構造を同定できるようになってきていますが、その大きさの結晶化すら困難なものがほとんどです。フェムト秒レーザーを用いることにより、このような有機分子やタンパク質の結晶化が高効率に行えることが示されており、今後の応用が期待されています。現在、フェムト秒レーザーにより有機分子・タンパク質が結晶化するメカニズムの探索を進めています。
主な報告とトピックス
>>>PageTopタンパク質パターニング(プロテインチップの作製)

レーザートラッピングとフェムト秒レーザー誘起衝撃波を駆使して、プロテインチップの作製を試みています。プロテインチップとは特定の機能を持ったタンパク質を基板上に配列した素子のことです。タンパク質は非常に柔らかく、豆腐とかヨーグルトみたいなもので、簡単に基板に貼り付けることはできません。さらにタンパク質は一端乾いてしまうとその性質が変化してしまいます。例えば、バブルジェットプリンターの印刷機を使ってタンパク質を印刷しても、固着の際に乾燥してしまうので、印刷されたタンパク質の性質は変わってしまいます。この様な問題を克服するために、レーザートラッピングやフェムト秒レーザー誘起衝撃波を用いて水溶液中でタンパク質の微結晶を配列し、接着する方法を提案しています。
主な報告とトピックス
>>>PageTop細胞パターニング

フェムト秒レーザー誘起衝撃波を駆使して、単一レベルの細胞を高速かつ高精度に配列する方法を開発しています。生体機能を部分的に模した生体デバイスの高集積化にあたり、多種類の細胞を、安定かつ自在に、高精度かつ迅速に配置する技術の確立が望まれています。このような配列手法として、インクジェットプリンティングやマイクロコンタクトプリンティングによる方法が検討されていますが、配置精度の向上や配置する生体材料の安定性の向上が課題となっています。私たちは、水のフェムト秒レーザーアブレーションを利用した複数種類の細胞を配列する独自の方法を考案し、オールウエットプロセスにおいて秒速90
mm以上で100 mmの線幅で細胞を生きたまま配列することに成功しています。